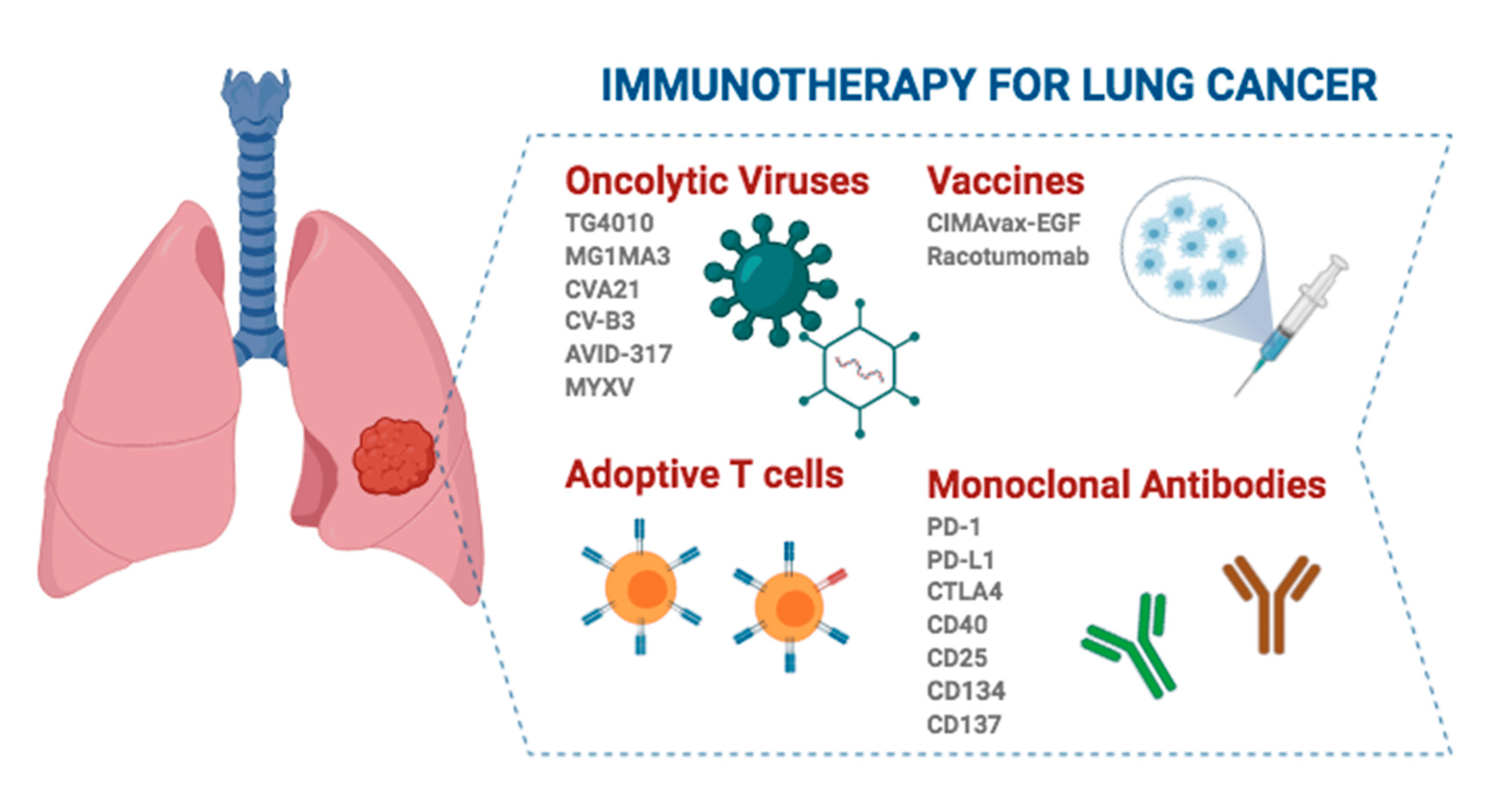
फोक्सोको क्यान्सरको कुल संख्याको लगभग ८०%-८५% गैर-सानो कोशिका फोक्सोको क्यान्सर (NSCLC) हो, र प्रारम्भिक NSCLC को कट्टरपन्थी उपचारको लागि शल्यक्रिया रिसेक्सन सबैभन्दा प्रभावकारी माध्यम हो। यद्यपि, पुनरावृत्तिमा केवल १५% कमी र पेरिऑपरेटिभ केमोथेरापी पछि ५ वर्षको बाँच्नमा ५% सुधारको साथ, त्यहाँ एक ठूलो अपरिपक्व क्लिनिकल आवश्यकता छ।
हालैका वर्षहरूमा NSCLC को लागि पेरियोपरेटिभ इम्युनोथेरापी एउटा नयाँ अनुसन्धान केन्द्र हो, र धेरै चरण ३ को अनियमित नियन्त्रित परीक्षणहरूको नतिजाले पेरियोपरेटिभ इम्युनोथेरापीको महत्त्वपूर्ण स्थान स्थापित गरेको छ।
सञ्चालनयोग्य प्रारम्भिक चरणको गैर-सानो कोशिका फोक्सोको क्यान्सर (NSCLC) भएका बिरामीहरूको लागि इम्युनोथेरापीले हालका वर्षहरूमा उल्लेखनीय प्रगति गरेको छ, र यो उपचार रणनीतिले बिरामीहरूको बाँच्ने क्षमता मात्र बढाउँदैन, तर परम्परागत शल्यक्रियाको लागि प्रभावकारी पूरक प्रदान गर्दै जीवनको गुणस्तर पनि सुधार गर्दछ।
इम्युनोथेरापी कहिले दिइन्छ भन्ने आधारमा, सञ्चालनयोग्य प्रारम्भिक चरणको NSCLC को उपचारमा इम्युनोथेरापीका तीन मुख्य ढाँचाहरू छन्:
१. नियोएडजुभेन्ट इम्युनोथेरापी मात्र: ट्युमरको आकार घटाउन र पुनरावृत्तिको जोखिम कम गर्न शल्यक्रिया अघि इम्युनोथेरापी गरिन्छ। चेकमेट ८१६ अध्ययन [१] ले केमोथेरापीसँग मिलाएर इम्युनोथेरापीले केमोथेरापीको तुलनामा नियोएडजुभेन्ट चरणमा घटना-मुक्त बाँच्ने (EFS) मा उल्लेखनीय सुधार गरेको देखाएको छ। थप रूपमा, नियोएडजुभेन्ट इम्युनोथेरापीले बिरामीहरूको प्याथोलोजिकल पूर्ण प्रतिक्रिया दर (pCR) मा सुधार गर्दै पुनरावृत्ति दरलाई पनि कम गर्न सक्छ, जसले गर्दा शल्यक्रियापछि पुनरावृत्तिको सम्भावना कम हुन्छ।
२. पेरियोपरेटिभ इम्युनोथेरापी (नियोएडजुभेन्ट + एडजुभेन्ट): यस मोडमा, शल्यक्रिया अघि र पछि इम्युनोथेरापी गरिन्छ ताकि यसको एन्टीट्युमर प्रभाव अधिकतम होस् र शल्यक्रिया पछिको न्यूनतम अवशिष्ट घावहरू हटाइयोस्। यस उपचार मोडेलको मुख्य लक्ष्य नियोएडजुभेन्ट (पूर्व-शल्यक्रिया) र सहायक (अपरेटिभ पछि) चरणहरूमा इम्युनोथेरापी संयोजन गरेर ट्यूमर बिरामीहरूको दीर्घकालीन बाँच्ने र उपचार दर सुधार गर्नु हो। कीकीनोट ६७१ यस मोडेलको प्रतिनिधि हो [२]। सकारात्मक EFS र OS अन्त्य बिन्दुहरूको साथ एक मात्र अनियमित नियन्त्रित परीक्षण (RCT) को रूपमा, यसले पेरियोपरेटिभली रिसेक्टेबल चरण Ⅱ, ⅢA, र ⅢB (N2) NSCLC बिरामीहरूमा केमोथेरापीसँग संयुक्त पालिजुम्याबको प्रभावकारिताको मूल्याङ्कन गर्यो। केमोथेरापीको तुलनामा, केमोथेरापीसँग संयुक्त पेम्ब्रोलिजुम्याबले मध्य EFS लाई २.५ वर्षले विस्तार गर्यो र रोगको प्रगति, पुनरावृत्ति, वा मृत्युको जोखिम ४१% ले घटायो; KEYNOTE-671 पनि पहिलो इम्युनोथेरापी अध्ययन थियो जसले रिसेक्टेबल NSCLC मा समग्र बाँच्ने (OS) लाभ प्रदर्शन गर्यो, मृत्युको जोखिममा २८% कमी (HR, ०.७२), सञ्चालनयोग्य प्रारम्भिक-चरण NSCLC को लागि नियोएडजुभ्यान्ट र सहायक इम्युनोथेरापीमा एक कोसेढुङ्गा।
३. सहायक इम्युनोथेरापी मात्र: यस मोडमा, बिरामीहरूले शल्यक्रिया अघि औषधि उपचार प्राप्त गरेनन्, र अवशिष्ट ट्युमरहरूको पुनरावृत्ति रोक्न शल्यक्रिया पछि इम्युनोड्रगहरू प्रयोग गरिन्थ्यो, जुन उच्च पुनरावृत्ति जोखिम भएका बिरामीहरूको लागि उपयुक्त छ। IMpower010 अध्ययनले पूर्ण रूपमा रिसेक्ट गरिएको चरण IB देखि IIIA (AJCC 7 औं संस्करण) NSCLC [3] भएका बिरामीहरूमा पोस्टअपरेटिभ सहायक एटिलिजुमाबको प्रभावकारिताको मूल्याङ्कन गर्यो। नतिजाहरूले देखाए कि एटिलिजुमाबको साथ सहायक थेरापीले चरण ⅱ देखि ⅢA मा PD-L1 सकारात्मक बिरामीहरूमा रोग-मुक्त बाँच्न (DFS) लाई उल्लेखनीय रूपमा लामो समयसम्म लम्ब्यायो। थप रूपमा, KEYNOTE-091/PEARLS अध्ययनले चरण IB देखि IIIA NSCLC [4] भएका पूर्ण रूपमा रिसेक्ट गरिएका बिरामीहरूमा सहायक थेरापीको रूपमा पेम्ब्रोलिजुमाबको प्रभावको मूल्याङ्कन गर्यो। समग्र जनसंख्यामा पाबोलिजुमाब उल्लेखनीय रूपमा लामो समयसम्म रह्यो (HR, ०.७६), पाबोलिजुमाब समूहमा ५३.६ महिना र प्लेसिबो समूहमा ४२ महिनाको औसत DFS सहित। PD-L1 ट्युमर अनुपात स्कोर (TPS) ≥५०% भएका बिरामीहरूको उपसमूहमा, यद्यपि पाबोलिजुमाब समूहमा DFS लामो समयसम्म रह्यो, दुई समूहहरू बीचको भिन्नता तुलनात्मक रूपमा सानो नमूना आकारको कारणले तथ्याङ्कीय रूपमा महत्त्वपूर्ण थिएन, र पुष्टि गर्न लामो फलो-अप आवश्यक थियो।
इम्युनोथेरापीलाई अन्य औषधिहरूसँग जोड्ने वा उपचारात्मक उपायहरू र संयोजन मोड अनुसार, नियोएडजुभेन्ट इम्युनोथेरापी र एडजुभेन्ट इम्युनोथेरापीको कार्यक्रमलाई निम्न तीन मुख्य मोडहरूमा विभाजन गर्न सकिन्छ:
१. एकल इम्युनोथेरापी: यस प्रकारको थेरापीमा LCMC3 [5], IMpower010 [3], KEYNOTE-091/PEARLS [4], BR.31 [6], र ANVIL [7] जस्ता अध्ययनहरू समावेश छन्, जसमा (नयाँ) सहायक थेरापीको रूपमा एकल इम्युनोथेरापी औषधिहरूको प्रयोगद्वारा विशेषता दिइएको छ।
२. इम्युनोथेरापी र केमोथेरापीको संयोजन: यस्ता अध्ययनहरूमा KEYNOTE-671 [2], CheckMate 77T [8], AEGEAN [9], RATIONALE-315 [10], Neotorch [11], र IMpower030 [12] समावेश छन्। यी अध्ययनहरूले पेरिऑपरेटिभ अवधिमा इम्युनोथेरापी र केमोथेरापीको संयोजनको प्रभावलाई हेरे।
३. अन्य उपचार विधिहरूसँग इम्युनोथेरापीको संयोजन: (१) अन्य इम्युनोड्रगहरूसँग संयोजन: उदाहरणका लागि, NEOSTAR परीक्षण [१३] मा साइटोटोक्सिक T लिम्फोसाइट-सम्बद्ध एन्टिजेन ४ (CTLA-४) लाई संयोजन गरिएको थियो, NEO-Predict-Lung परीक्षण [१४] मा लिम्फोसाइट सक्रियता जीन ३ (LAG-३) एन्टिबडी संयोजन गरिएको थियो, र SKYSCRAPER १५ परीक्षणमा T सेल इम्युनोग्लोबुलिन र ITIM संरचनाहरूलाई संयोजन गरिएको थियो। TIGIT एन्टिबडी संयोजन [१५] जस्ता अध्ययनहरूले प्रतिरक्षा औषधिहरूको संयोजन मार्फत एन्टी-ट्युमर प्रभावलाई बढाएको छ। (२) रेडियोथेरापीसँग संयोजन गरिएको: उदाहरणका लागि, स्टेरियोट्याक्टिक रेडियोथेरापी (SBRT) सँग संयोजन गरिएको डुभलियम्याब प्रारम्भिक NSCLC [१६] को उपचारात्मक प्रभाव बढाउन डिजाइन गरिएको हो; (३) एन्टी-एन्जियोजेनिक औषधिहरूसँग संयोजन: उदाहरणका लागि, EAST ENERGY अध्ययन [१७] ले इम्युनोथेरापीसँग संयोजन गरिएको रमुमाबको सिनर्जिस्टिक प्रभावको अन्वेषण गर्यो। धेरै इम्युनोथेरापी मोडहरूको अन्वेषणले पेरियोपरेटिभ अवधिमा इम्युनोथेरापीको प्रयोग संयन्त्र अझै पूर्ण रूपमा बुझिएको छैन भनेर देखाउँछ। यद्यपि इम्युनोथेरापीले मात्र पेरियोपरेटिभ उपचारमा सकारात्मक नतिजा देखाएको छ, केमोथेरापी, विकिरण थेरापी, एन्टीएन्जियोजेनिक थेरापी, र CTLA-4, LAG-3, र TIGIT जस्ता अन्य प्रतिरक्षा चेकपोइन्ट अवरोधकहरूलाई संयोजन गरेर, अनुसन्धानकर्ताहरूले इम्युनोथेरापीको प्रभावकारितालाई अझ बढाउने आशा राखेका छन्।
सञ्चालनयोग्य प्रारम्भिक NSCLC को लागि इम्युनोथेरापीको इष्टतम मोडको बारेमा अझै पनि कुनै निष्कर्ष छैन, विशेष गरी पेरियोपरेटिभ इम्युनोथेरापी नियोएडजुभेन्ट इम्युनोथेरापीसँग मात्र तुलना गरिन्छ कि हुँदैन, र थप सहायक इम्युनोथेरापीले महत्त्वपूर्ण अतिरिक्त प्रभावहरू ल्याउन सक्छ कि सक्दैन, प्रत्यक्ष तुलनात्मक परीक्षण परिणामहरूको अभाव अझै पनि छ।
फोर्डे एट अलले अनियमित नियन्त्रित परीक्षणहरूको प्रभाव अनुकरण गर्न अन्वेषणात्मक प्रवृत्ति स्कोर भारित विश्लेषण प्रयोग गरे, र यी कारकहरूको भ्रामक प्रभाव कम गर्न विभिन्न अध्ययन जनसंख्याहरू बीच आधारभूत जनसांख्यिकी र रोग विशेषताहरू समायोजन गरे, जसले गर्दा चेकमेट ८१६ [१] र चेकमेट ७७टी [८] को नतिजाहरू तुलनात्मक भए। औसत अनुगमन समय क्रमशः २९.५ महिना (चेकमेट ८१६) र ३३.३ महिना (चेकमेट ७७टी) थियो, जसले EFS र अन्य प्रमुख प्रभावकारिता उपायहरू अवलोकन गर्न पर्याप्त अनुगमन समय प्रदान गर्यो।
भारित विश्लेषणमा, EFS को HR ०.६१ (९५% CI, ०.३९ देखि ०.९७) थियो, जसले निओएडजुभेन्ट नाबुल्युम्याब संयुक्त केमोथेरापी समूह (चेकमेट ७७T मोड) मा पुनरावृत्ति वा मृत्युको जोखिम ३९% कम देखाएको सुझाव दिन्छ। पेरियोएपरेटिभ नेबुल्युम्याब प्लस केमोथेरापी समूहले आधारभूत चरणमा सबै बिरामीहरूमा सामान्य फाइदा देखायो, र १% भन्दा कम ट्युमर PD-L1 अभिव्यक्ति भएका बिरामीहरूमा प्रभाव बढी स्पष्ट थियो (पुनरावृत्ति वा मृत्युको जोखिममा ४९% कमी)। थप रूपमा, pCR प्राप्त गर्न असफल भएका बिरामीहरूको लागि, पेरियोएपरेटिभ नाबुल्युम्याब संयुक्त केमोथेरापी समूहले निओएडजुभेन्ट नाबुल्युम्याब संयुक्त केमोथेरापी समूहको तुलनामा EFS को ठूलो फाइदा (पुनरावृत्ति वा मृत्युको जोखिममा ३५% कमी) देखायो। यी नतिजाहरूले सुझाव दिन्छ कि पेरियोपरेटिभ इम्युनोथेरापी मोडेल नियोएडजुभेन्ट इम्युनोथेरापी मोडेल भन्दा बढी लाभदायक छ, विशेष गरी कम PD-L1 अभिव्यक्ति र प्रारम्भिक उपचार पछि ट्युमर अवशेष भएका बिरामीहरूमा।
यद्यपि, केही अप्रत्यक्ष तुलनाहरू (जस्तै मेटा-विश्लेषणहरू) ले नियोएडजुभेन्ट इम्युनोथेरापी र पेरियोपरेटिभ इम्युनोथेरापी [18] बीचको बाँच्नमा कुनै महत्त्वपूर्ण भिन्नता देखाएको छैन। व्यक्तिगत बिरामी डेटामा आधारित मेटा-विश्लेषणले पत्ता लगायो कि पेरियोपरेटिभ इम्युनोथेरापी र नियोएडजुभेन्ट इम्युनोथेरापीले सञ्चालनयोग्य प्रारम्भिक-चरण NSCLC [19] भएका बिरामीहरूमा pCR र गैर-PCR उपसमूहहरूमा EFS मा समान परिणामहरू पाएका थिए। थप रूपमा, सहायक इम्युनोथेरापी चरणको योगदान, विशेष गरी बिरामीहरूले pCR प्राप्त गरेपछि, क्लिनिकमा एक विवादास्पद बिन्दु बनेको छ।
हालै, अमेरिकी खाद्य तथा औषधि प्रशासन (FDA) को ओन्कोलोजी ड्रग्स सल्लाहकार समितिले यस विषयमा छलफल गर्यो, सहायक इम्युनोथेरापीको विशिष्ट भूमिका अझै अस्पष्ट छ भन्ने कुरामा जोड दिँदै [20]। छलफल गरियो कि: (१) उपचारको प्रत्येक चरणको प्रभाव छुट्याउन गाह्रो छ: पेरिऑपरेटिभ कार्यक्रममा दुई चरणहरू, नियोएडजुभेन्ट र सहायक हुने भएकाले, समग्र प्रभावमा प्रत्येक चरणको व्यक्तिगत योगदान निर्धारण गर्न गाह्रो हुन्छ, जसले गर्दा कुन चरण बढी महत्वपूर्ण छ वा दुवै चरणहरू एकैसाथ सञ्चालन गर्न आवश्यक छ कि छैन भनेर निर्धारण गर्न गाह्रो हुन्छ; (२) अत्यधिक उपचारको सम्भावना: यदि दुवै उपचार चरणहरूमा इम्युनोथेरापी संलग्न छ भने, यसले बिरामीहरूलाई अत्यधिक उपचार प्राप्त गर्न र साइड इफेक्टको जोखिम बढाउन सक्छ; (३) बढेको उपचार बोझ: सहायक उपचार चरणमा थप उपचारले बिरामीहरूको लागि उच्च उपचार बोझ निम्त्याउन सक्छ, विशेष गरी यदि समग्र प्रभावकारितामा यसको योगदानको बारेमा अनिश्चितता छ भने। माथिको बहसको जवाफमा, स्पष्ट निष्कर्ष निकाल्नको लागि, भविष्यमा थप प्रमाणीकरणको लागि थप कडाइका साथ डिजाइन गरिएको अनियमित नियन्त्रित परीक्षणहरू आवश्यक पर्दछ।
पोस्ट समय: डिसेम्बर-०७-२०२४